Hallazgos clínicos demuestran que la inflamación y disfunción del sistema inmunológico mediada por la composición de la microbiota, son elementos clave en el desarrollo de problemas gastrointestinales y otras enfermedades extraintestinales como el Trastorno del Espectro Autista (TEA). Aunque la dieta puede ser la herramienta más poderosa para la modulación de la microbiota, metaanálisis que evalúan su efecto en esta población, concluyen que si bien existen indicios de la utilidad del abordaje alimentario, aún faltan estudios para lograr un nivel de evidencia que permita aconsejar a todos los pacientes.

Dra. Ileana C. Carzoglio Algazi, MSc
Doctora en Medicina, egresada de UDELAR 2005. *1
Lic. Nta. Paula Mendive Dubourdieu, MSc
Licenciada en Nutrición por la Universidad Complutense de Madrid. *2
La microbiota del cuerpo humano está formada por más de 1014 microorganismos presentes en diferentes áreas del organismo. El tracto gastrointestinal constituye la mayor interfase del huésped expuesta al medio externo y contiene aproximadamente dos tercios de la comunidad microbiana comensal humana. Aunque la microbiota intestinal (MI) incluye virus, hongos, protozoos, arqueas y bacterias, el componente bacteriano es el más estudiado.
Los principales filos bacterianos de la MI incluyen Firmicutes, Bacteroidetes, Actinobacterias y Proteobacterias. El uso creciente de la tecnología de secuenciación profunda de alto rendimiento en la última década, ha revelado que el microbioma intestinal codifica 3,3 millones de genes, 100 veces más que el número de genes humanos. Por este motivo, el microbioma intestinal también se denomina “segundo genoma humano”.
Los componentes de la MI se dividen en tres grupos de acuerdo con sus funciones: microorganismos benéficos comensales, patógenos potencialmente sensibles y bacterias patógenas. Los microorganismos comensales “beneficiosos” mantienen un ambiente saludable en el huésped y ofrecen beneficios, además de interactuar con los tejidos de una manera cooperativa y no patogénica. A esto le llamamos “Eubiosis”.
Estudios de taxonomía demuestran que incluso en poblaciones humanas homogéneas, hay pocas bacterias comunes, existiendo incluso variabilidad individual en diferentes días, por lo que adquiere mayor relevancia la capacidad funcional y metabólica de la microbiota.[1] El novedoso concepto de “holobionte” comprende al ser humano y a la microbiota que lo habita.
Son múltiples las patologías vinculadas actualmente a la disbiosis intestinal y al intestino hiper-permeable (leaky gut). Los avances en el desarrollo, asociado a la reducción de costos para la investigación en diferentes patologías, han permitido identificar nuevos “ejes intestino-órgano específicos”, de los cuales el eje Intestino-Cerebro es el más estudiado.[2]
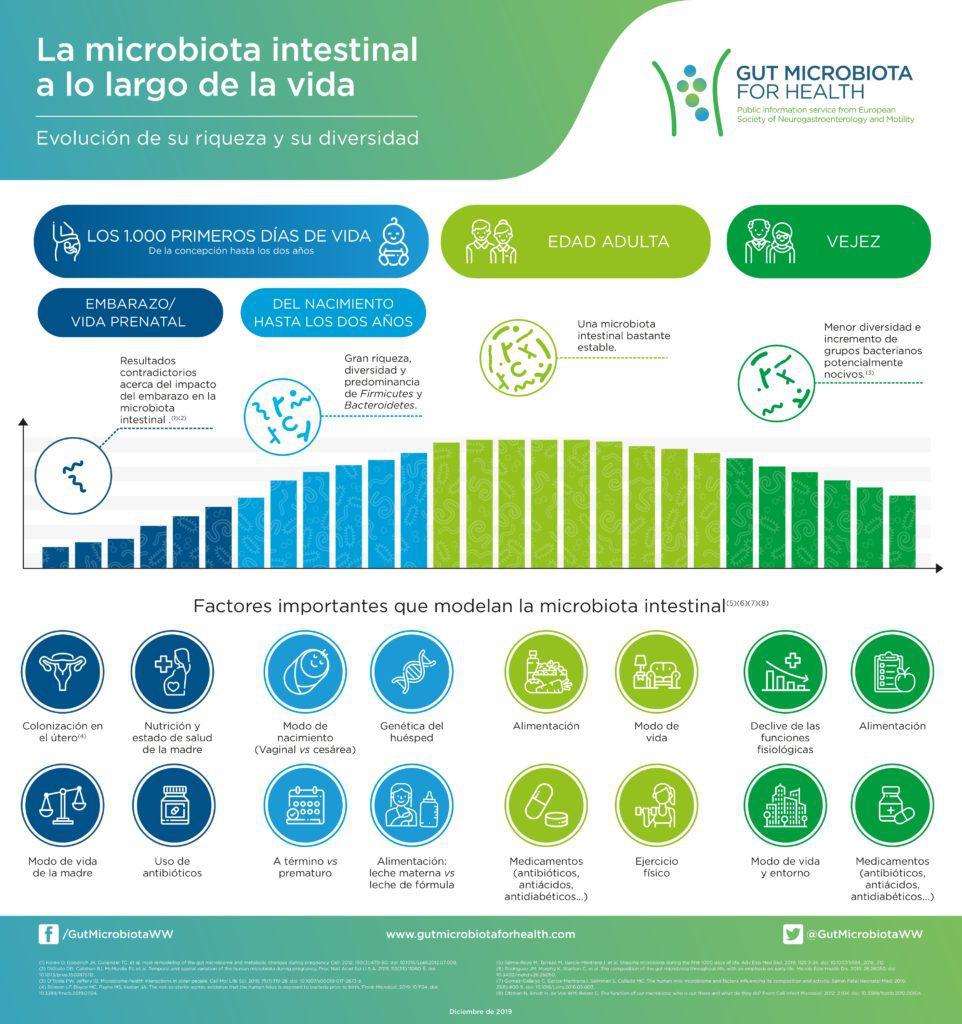
El establecimiento y desarrollo de una composición beneficiosa de la microbiota ocurre durante los primeros mil días de vida. Esta ventana temporal es crucial en la programación y desarrollo de los sistemas inmunológico y nervioso.
Factores ambientales y parentales como la genética del huésped, la salud mental, la nutrición, el modo de nacer (parto/cesárea) y alimentación, la exposición a antibióticos, la activación inmunitaria y la composición de la microbiota prenatal, pueden modular la composición de la microbiota de la madre y del bebé. De todos estos factores, la nutrición en la vida temprana juega un papel fundamental en la programación perinatal y en la modulación de la microbiota de la descendencia. Perturbaciones en esta etapa crítica tiene efectos duraderos en el eje microbiota-intestino-cerebro.[3]
Según los hallazgos clínicos, la inflamación y disfunción del sistema inmunológico mediada por la composición de la microbiota, son elementos clave en el desarrollo de problemas gastrointestinales y otras enfermedades extraintestinales como el Trastorno del Espectro Autista (TEA).
La disbiosis en estos niños se ha relacionado no solo con el problema gastrointestinal habitualmente comórbido, sino también con la intensidad de la sintomatología autista, lo que sugiere que la actividad bacteriana y los metabolitos resultantes están involucrados en el desarrollo y severidad del TEA. Estos hallazgos son la base del concepto “eje microbioma-intestino-cerebro” que postula que existe una interacción bidireccional entre las bacterias intestinales y el cerebro.
Si bien se sabe que esta comunicación se produce por medio de hormonas y neurotransmisores liberados por el sistema endocrino intestinal en función de la microbiota y metabolitos que existan, los mecanismos subyacentes específicos de esta interacción fisiológica no están del todo claros y hace falta más investigación para lograr una mejor comprensión sobre la comunicación fisiológica entre el intestino y el cerebro. Más aún, todavía se está estudiando la dirección de la causalidad, es decir, si las alteraciones en la microbiota provocan inflamación y desequilibrios en el sistema inmunológico o viceversa.
De todas maneras, en comparación con niños neurotípicos, los niños con TEA muestran una mayor abundancia de Bacteroidetes (Bacteroides y Parabacteroides) y algunos géneros del filo Firmicutes (específicamente Clostridium, Faecalibacterium y Phascolarctobacterium) junto con una menor abundancia de Coprococcus y Bifidobacterias.
Las bacterias formadoras de esporas, como Clostridium, liberan toxinas proinflamatorias que pueden llegar al cerebro por vía sanguínea y se han asociado con comportamientos repetitivos y alteraciones gastrointestinales en el TEA. Por otro lado, los ácidos grasos de cadena corta (AGCC) participan en el funcionamiento adecuado del sistema inmunológico intestinal mediante la modulación de la expresión génica. Cualquier desequilibrio en su concentración puede alterar la homeostasis intestinal y desencadenar inflamación periférica. También, éstos llegan al cerebro por vía sanguínea e influyen en su desarrollo al modular la producción de serotonina y dopamina. En este sentido, el ácido propiónico (PPA) producido principalmente por Bacteroidetes, es uno de los principales AGCC neurotóxicos cuando aumenta su concentración. Faecalibacterium está relacionado con la regulación del interferón (IFN) gamma que desempeña un papel indirecto en la plasticidad cerebral y la formación de las sinapsis.
Los cambios en la microbiota pueden alterar la señalización cerebral, induciendo algunos comportamientos de TEA al cambiar las concentraciones de IFN-gamma. Algunas especies de Bifidobacterium producen GABA, cuyas concentraciones se han encontrado bajas en niños con TEA. Los GABA están estrechamente relacionados con el metabolismo del glutamato, que es el principal neurotransmisor excitatorio del cerebro. Anomalías de GABA / glutamato podrían desempeñar un papel importante en la patología de los niños con TEA.
Asimismo, se han encontrado alteraciones del metabolismo del triptófano (Trp), precursor de la serotonina, un neurotransmisor involucrado en casi todos los comportamientos, incluidos el apetito, el sueño, las emociones y las habilidades cognitivas y sociales.
También, comparado con niños neurotípicos, se han observado en niños con TEA niveles más bajos de glutatión, homocisteína, metionina y S-adenosilmetionina. Algunos de éstos están implicados en el metabolismo del azufre y la metilación, que contribuyen a la reducción del estrés oxidativo, la desintoxicación celular y la excreción de metales pesados. La desregulación de aminoácidos en los niños con TEA podría, por lo tanto, ser otro mecanismo subyacente al desarrollo y la gravedad de la sintomatología autista.[4]
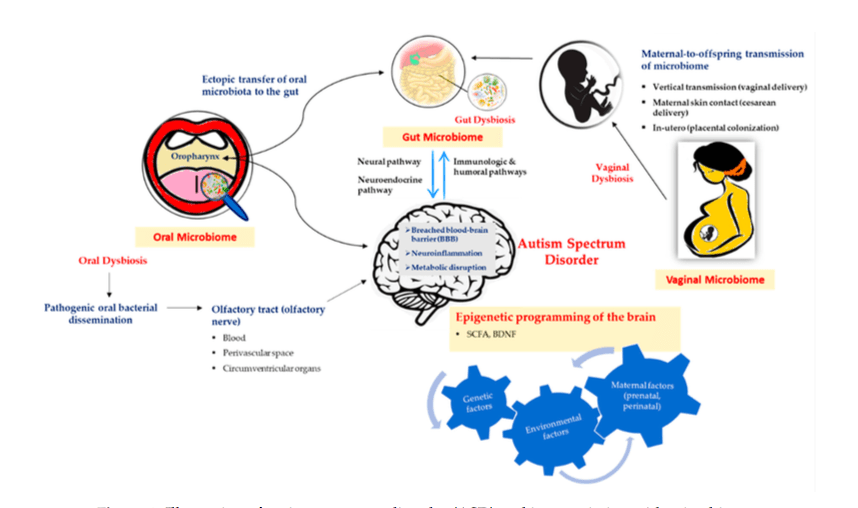
La figura siguiente ilustra el posible mecanismo involucrado en la interacción microbioma-cerebro en el contexto del trastorno del TEA. Las vías neural, neuroendocrina e inmunológica y humoral son los mediadores potenciales en la comunicación bidireccional en este eje. La contribución materna es significativa en la determinación de la colonización intestinal temprana en la descendencia, mientras que, en general, los factores ambientales que alteran significativamente el microbioma materno durante los períodos prenatal y perinatal influyen en la composición microbiana de la descendencia.
Se cree que otra vía de intercambio posible en el eje intestino-cerebro está mediada por la orofaringe, que tiene un papel importante en la patología del TEA.
Algunas investigaciones indican que la malnutrición por exceso (sobrepeso/obesidad) son más frecuentes en niños con TEA.[5] La selectividad alimentaria y los hábitos alimentarios característicos de estos niños parecen resultar en una deficiencia de algunos micronutrientes,[6] con una ingesta significativamente menor de proteínas, calcio, fósforo, selenio, vitamina D, tiamina, riboflavina y vitamina B12, y una ingesta mayor de ácidos grasos poliinsaturados y vitamina E, menor ingesta de omega-3 y mayor de frutas y verduras, comparado con niños neurotípicos.[7]
En suma, el TEA es uno de los trastornos del desarrollo neurológico que se ha explorado más en relación con el microbioma intestinal. La utilización del conocimiento microbiano, promete una perspectiva más integradora en la comprensión de este trastorno, aunque es un campo emergente en la investigación. Las intervenciones basadas en la microbiota incluyen: dieta, prebióticos, probióticos, antibióticos y trasplante microbiano fecal (TMF).[8]
La administración temprana de probióticos puede reducir el riesgo de desarrollo del TEA.[9] Ensayos clínicos con probióticos que contienen cepas de Lactobacillus y Bifidobacterium han informado de mejoras en el estado de ánimo, la ansiedad, la calidad del sueño y la depresión.[10] El TMF también parece mejorar la diversidad bacteriana al aumentar significativamente la abundancia de Bifidobacterium, Desulfovibrio y Prevotella[11] que persiste a los 24 meses.[12]
La dieta es probablemente la herramienta más poderosa para la modulación de la microbiota y aprender a utilizarla para generar una microbiota saludable debe ser una prioridad. Es importante prevenir factores de riesgo como la obesidad, el bajo peso, los déficits de vitaminas, así como detectar hipo o hipertiroidismo y la dislipemia, ya que su tratamiento contribuiría a mejorar la calidad de vida del paciente y la familia.[13] En la medida en que comprendamos mejor las interacciones dieta-huésped-microbiota, podremos capitalizar una verdadera medicina preventiva y personalizada.[14]
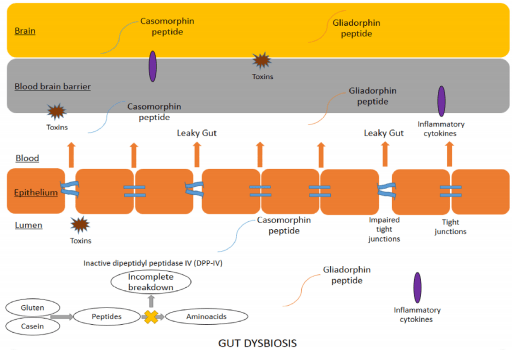
Se sugirió por primera vez en la década de 1980 que el consumo de alimentos que contienen proteínas como el gluten y la caseína podía causar síntomas parecidos al autismo por alteración de las funciones cerebrales.[15] La caseína es una de las proteínas que con gran frecuencia causa reacciones inmunológicas en los niños. En un estudio se vio que los niños con TEA que siguen la dieta libre de gluten y caseína (GFCF) tienen menos factor de necrosis tumoral-α (TNF-α) que los que no realizan la dieta.[16]
En niños con TEA se ha reportado que, péptidos digeridos de forma incompleta atraviesan la mucosa intestinal hiperpermeable y por vía sanguínea, atravesando la barrera hematoencefálica llegan al sistema nervioso central y tienen efectos negativos en la atención, maduración, comunicación social y aprendizaje.[17]
Desde hace 50 años el Autism Research Institute[18] en California y en la misma línea LINCA (Liga de Intervención Nutricional en Autismo y Trastorno por Déficit Atencional e Hiperactividad-TDAH) desde el año 2000 en México[19], promueven la prueba terapéutica en niños con TEA y TDAH de la dieta de exclusión de gluten, caseína y soja, baja en azúcares, así como la suplementación en nutrientes deficitarios, ya que continúa reportando mejoría de los síntomas gastrointestinales, neurológicos, comportamentales así como de los trastornos del sueño y la hiperactividad en algunos pacientes.
Las dificultades para generar evidencia científica sólida en este abordaje, radica no solo en la falta de fondos para este tipo de estudios, que en general terminan abarcando poblaciones pequeñas de niños, sino también en lo heterogéneo del trastorno, así como su abordaje terapéutico desde múltiples disciplinas, lo que vuelve más complejo el estudio cuando se quiere comparar con casos control. Los metaanálisis que evalúan el efecto de la dieta continúan concluyendo que si bien hay indicios de que podría ser útil este abordaje alimentario, hacen falta más estudios para lograr el suficiente nivel de evidencia como para aconsejar a todos los pacientes.
Los niños con TEA muestran una mayor abundancia de Bacteroidetes (Bacteroides y Parabacteroides) y algunos géneros del filo Firmicutes (específicamente Clostridium, Faecalibacterium y Phascolarctobacterium), junto con una menor abundancia de Coprococcus y Bifidobacterias.
[1] Qin J. et al. A human gut microbial gene catalogue established by metagenomic sequencing. Nature 2010 (464):59–65. https://doi.org/10.1038/nature08821.
[2] Ahlawat S et al. Gut–organ axis: a microbial outreach and networking. Lett Appl Microbiol. 2020. https://doi.org/10.1111/lam.13333.
[3] Ratsika, Anna et al. Priming for Life: Early Life Nutrition and the Microbiota-Gut-Brain Axis. Nutrients vol. 13,2 423. 28 Jan. 2021, doi:10.3390/nu13020423
[4] Iglesias-Vázquez, Lucía et al. Composition of Gut Microbiota in Children with Autism Spectrum Disorder: A Systematic Review and Meta-Analysis. Nutrients vol. 12,3 792. 17 Mar. 2020, doi:10.3390/nu12030792
[5] Shmaya Y, et al. Nutritional deficiencies and overweight prevalence among children with autism spectrum disorder. Res Dev Disabil. 2015;38:1–6. doi:10.1016/j.ridd.2014.11.020
[6] Tomova, Aleksandra et al. The Influence of Food Intake Specificity in Children with Autism on Gut Microbiota. International journal of molecular sciences vol. 21,8 2797. 17 Apr. 2020, doi:10.3390/ijms21082797
[7] Esteban-Figuerola, Patricia et al. Differences in food consumption and nutritional intake between children with autism spectrum disorders and typically developing children: A meta-analysis. Autism : the international journal of research and practice vol. 23,5 (2019): 1079-1095. doi:10.1177/1362361318794179
[8] Johnson, Dinyadarshini et al. A Revolutionizing Approach to Autism Spectrum Disorder Using the Microbiome. Nutrients vol. 12,7 1983. 3 Jul. 2020, doi:10.3390/nu12071983
[9] Partty A et al. A possible link between early probiotic intervention and the risk of neuropsychiatric disorders later in child- hood: a randomized trial. Pediatric Research, vol. 77, no. 6, pp. 823–828, 2015.
[10] Marotta, A. et al. Effects of probiotics on cognitive reactivity, mood, and sleep quality. Front. Psychiatry 2019, 10, 164.
[11] Xu, Hao-Ming et al. Fecal Microbiota Transplantation: A New Therapeutic Attempt from the Gut to the Brain. Gastroenterology research and practice vol. 2021 6699268. 16 Jan. 2021, doi:10.1155/2021/6699268
[12] Kang, Dae-Wook et al. Long-term benefit of Microbiota Transfer Therapy on autism symptoms and gut microbiota. Scientific reports vol. 9,1 5821. 9 Apr. 2019, doi:10.1038/s41598-019-42183-0
[13] Muskens J. B. et al. Medical comorbidities in children and adolescents with autism spectrum disorders and attention deficit hyperactivity disorders: a systematic review. European Child & Adolescent Psychiatry, 2017; 26(9), 1093–1103. doi:10.1007/s00787-017-1020-0
[14] Moles, Laura, and David Otaegui. The Impact of Diet on Microbiota Evolution and Human Health. Is Diet an Adequate Tool for Microbiota Modulation?. Nutrients vol. 12,6 1654. 2 Jun. 2020, doi:10.3390/nu12061654
[15] Ciéslińska A, Kostyra E, Savelkoul HFJ. Treating autism spectrum disorder with gluten-free and casein-free diet: the underlying microbiota-gutbrain axis mechanisms. HSOA Journal of Clinical Immunology and Immunotherapy 2017; 3. https://edepot.wur.nl/432879
[16] Sampson HA, Anderson JA. Summary and recommendations: classification of gastrointestinal
manifestations due to immunologic reactions to foods in infants and young children. J Pediatr Gastroenterol Nutr 2000; 30: S87-94.
[17] Baspinar B, Yardimci H. Gluten-Free Casein-Free Diet for Autism Spectrum Disorders: Can It Be Effective in Solving Behavioural and Gastrointestinal Problems? Eurasian J Med. 2020 Oct;52(3):292-297. doi: 10.5152/eurasianjmed.2020.19230. Epub 2020 Jun 4. PMID: 33209084; PMCID: PMC7651765.

